Fique por dentro das novidades
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!
Questão ativa
Já visualizadas
Não visualizadas
Resolução pendente
Questão anulada
Sem alternativas

Considere os dados a seguir de eletronegatividade de Pauling.
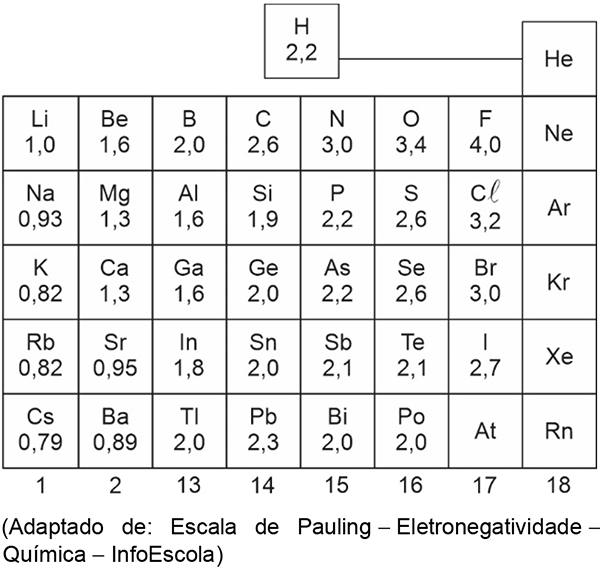
A ordem crescente de caráter iônico para os compostos LiC, NaF, KI e MgO é:
NaF < MgO < LiC < KI
NaF < LiC < MgO < KI
KI < MgO < LiC < NaF
MgO < KI < LiC < NaF
KI < NaF < MgO < LiC
Inicialmente, calcula-se a diferença de eletronegatividade (DE) dos elementos químicos envolvidos em cada uma das fórmulas químicas apresentadas. Assim:
DE (LiC𝓵) = 3,20 – 1,00 = 2,20
DE (NaF) = 4,00 – 0,93 = 3,07
DE (KI) = 2,70 – 0,82 = 1,88
DE (MgO) = 3,40 – 1,30 = 2,10
Quanto maior a diferença de eletronegatividade (DE), maior o caráter iônico da ligação química analisada.
Dessa forma, a ordem crescente de caráter iônico (e de DE) é: .
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!