Fique por dentro das novidades
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!
Questão ativa
Já visualizadas
Não visualizadas
Resolução pendente
Questão anulada
Sem alternativas

Analise a tabela que fornece valores de constantes de dissociação () de dois ácidos e () de duas bases a 25 °C.
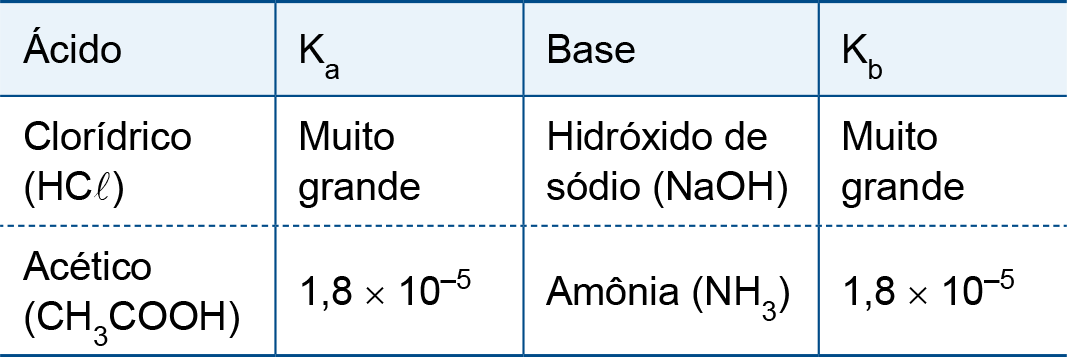
Considere quatro soluções aquosas 0,1 mol/L dos sais formados pelas reações entre os ácidos e bases citados na tabela:
1. NaC
2. Na()
3. ()
4.
Dentre essas soluções, duas que apresentam pH aproximadamente igual a 7 são as de números
1 e 3.
1 e 4 .
1 e 2.
2 e 3.
3 e 4.
1) NaC — sal de ácido forte (HC) e base forte (NaOH). Íons Cl⁻ e Na⁺ não sofrem hidrólise. Solução aproximadamente neutra: pH ≈ 7.
2) — sal de base forte (NaOH) e ácido fraco (). O ânion acetato () sofre hidrólise básica: . Solução básica (pH > 7).
3) — sal de ácido fraco () e base fraca (). Ambos os íons sofrem hidrólise: e . Como Ka (ácido fraco) = Kb (base fraca), as hidrólises se compensam e o pH fica aproximadamente 7.
4) — sal de ácido forte () e base fraca (). O cátion amônio () sofre hidrólise ácida: . Solução ácida (pH < 7).
Conclusão: as soluções aproximadamente neutras são as de números 1 e 3.
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!