Fique por dentro das novidades
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!
Questão ativa
Já visualizadas
Não visualizadas
Resolução pendente
Questão anulada
Sem alternativas

Diante das mudanças climáticas, muitos químicos desempenham um papel estratégico no enfrentamento desse problema. Uma dessas ações é o esforço no desenvolvimento de recursos que removem por meio da captura direta do ar. Nesse sentido, os químicos se dedicam a produzir materiais que, ao mesmo tempo, possam capturar o em situações diversas em quantidades e velocidades altas. Um exemplo disso é a captura cumulativa de (em mmol) por grama de tetraperoxotitanato de potássio em função do tempo. Esses resultados são parcialmente mostrados no gráfico a seguir.
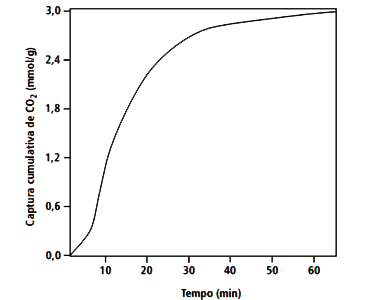
(Adaptado de BACH, K. et al. ChemRxiv, DOI: 10.26434/chemrxiv-2024-xb06z-v2. Acesso em 09/10/2025.)
Considerando as informações do gráfico, é correto afirmar que após 65 minutos de adsorção: (i) a razão molar [mol por mol de ] e (ii) o aumento percentual de massa do sólido serão aproximadamente de
Dado parcial: Massa molar:
(i) 3 e (ii) 13% em relação ao inicial.
(i) 1 e (ii) 13% em relação ao inicial.
(i) 3 e (ii) 30% em relação ao inicial.
(i) 1 e (ii) 30% em relação ao inicial.
Com base na análise do gráfico, verifica-se que, após 65 minutos de adsorção, a quantidade de adsorvida é de aproximadamente 3 mol por grama de tetraperoxotitanato de potássio.
A massa de 1 g de tetraperoxotitanato de potássio pode ser convertida para quantidade de matéria utilizando o dado da massa molar fornecido como:
A quantidade de matéria adsorvida de pode ser convertida para massa utilizando a massa molar calculada a partir da tabela periódica:
Com esses valores, podem-se realizar os cálculos solicitados pela questão.
(i) razão molar [mol por mol de ]:
(ii) aumento percentual de massa do sólido:
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!