Fique por dentro das novidades
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!

Para a neutralização de 0,18 g de um ácido carboxílico, são gastos 30 mL de uma solução 0,1 M de NaOH. A densidade do vapor deste ácido é trinta vezes a do hidrogênio, nas mesmas condições.
Considerando a dissociação completa desse ácido, forneça seu nome e sua estrutura molecular.
Dado que se trata de um ácido carboxílico, sua fórmula molecular é dada por .
A massa molar do ácido é calculada pela relação entre as densidades na fase gasosa:
Da titulação ácido-base, tem-se a proporção estequiométrica:
Assim, tem-se um monoácido, que apresentará somente uma carboxila . Portanto, sua fórmula molecular fica: .
Por inspeção: . Logo, tem-se: .
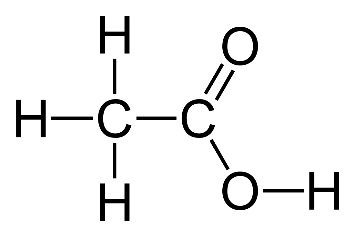
Trata-se, portanto, do ácido etanoico, cuja estrutura molecular é dada por:
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!