Fique por dentro das novidades
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!

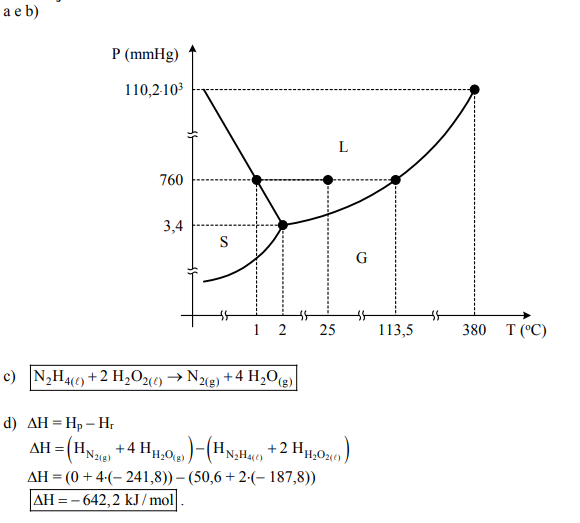
Um dos sistemas propelentes usados em foguetes consiste de uma mistura de hidrazina () e peróxido de hidrogênio (). Sabendo que o ponto triplo da hidrazina corresponde à temperatura de 2,0 °C e à pressão de 3,4 mmHg, que o ponto crítico corresponde à temperatura de 380 °C e à pressão de 145 atm e que na pressão de 1 atm as temperaturas de fusão e de ebulição são iguais a 1,0 e 113,5 °C, respectivamente, pedem-se:
a) Um esboço do diagrama de fases da hidrazina para o intervalo de pressão e temperatura considerados neste enunciado.
b) A indicação, no diagrama esboçado no item a), de todos os pontos indicados no enunciado e das fases presentes em cada região do diagrama.
c) A equação química completa e balanceada que descreve a reação de combustão entre hidrazina e peróxido de hidrogênio, quando estes são misturados numa temperatura de 25 °C e pressão de 1 atm. Nesta equação, indique os estados físicos de cada substância.
d) O cálculo da variação de entalpia da reação mencionada em c).
Dados eventualmente necessários: variação de entalpia de formação (), na temperatura de 25 °C e pressão de 1 atm, referem-se a:
(g) : = 95,4 kJ .
(l) := 50,6 kJ .
(l) := –187,8 kJ .
(g) : = –241,8 kJ .
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!