Fique por dentro das novidades
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!

São fornecidas as seguintes informações a respeito de titulação ácido-base:
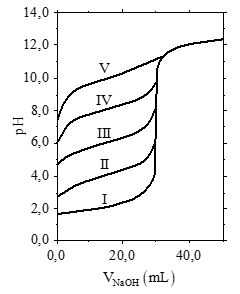
a) A figura mostra as curvas de titulação de 30,0 mL de diferentes ácidos (I, II, III, IV e V), todos a 0,10 mol L–1, com uma solução aquosa 0,10 mol L–1 em NaOH.
b) O indicador fenolftaleína apresenta o intervalo de mudança de cor entre pH 8,0 a 10,0, e o indicador vermelho de metila, entre pH 4,0 a 6,0.
Considerando estas informações, é CORRETO afirmar que
o indicador vermelho de metila é mais adequado que a fenolftaleína para ser utilizado na titulação do ácido IV.
o indicador vermelho de metila é mais adequado que a fenolftaleína para ser utilizado na titulação do ácido V.
o ácido III é mais forte que o ácido II.
os dois indicadores (fenolftaleína e vermelho de metila) são adequados para a titulação do ácido I.
os dois indicadores (fenolftaleína e vermelho de metila) são adequados para a titulação do ácido III.
A análise dos valores iniciais de pH nas soluções ácidas permite concluir que a ordem crescente de acidez é dada por:
V < IV < III < II < I
Na titulação de um ácido forte por uma base forte, a faixa de pH na “viragem” (ponto de equivalência) é muito ampla, razão pela qual podem ser usados indicadores que mudam de cor em pH variados.
Para ácidos fracos, será mais indicado o uso da fenolftaleína, uma vez que o sal formado sofre hidrólise, resultando solução básica.
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!