Fique por dentro das novidades
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!

Considere o diagrama de fase hipotético representado esquematicamente na figura ao lado: O que representam os pontos A, B, C, D e E?
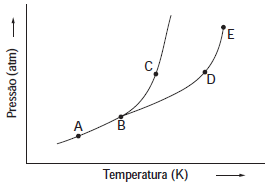
De acordo com o diagrama representado, tem-se:
– Ponto A: trata-se de um ponto da curva de sublimação em que coexistem, em equilíbrio, os estados sólido e vapor da substância analisada.
– Ponto B: é o conhecido ponto triplo, que consiste em uma condição específica de pressão e temperatura em que se tem a substância estudada em seus três estados físicos, em equilíbrio: sólido, líquido e vapor.
– Ponto C: trata-se de um ponto da curva de fusão, situação em que coexistem os estados sólido e líquido da substância, em equilíbrio.
– Ponto D: representa um ponto da curva de vaporização, que se caracteriza pelo equilíbrio entre os estados líquido e vapor da substância estudada.
– Ponto E: trata-se do ponto crítico da substância, ou seja, as condições de pressão e temperatura limites, a partir das quais não há mais distinção entre os estados líquido e vapor.
Poliedro Resolve ITA 2013 - Química
Inscreva-se em nossa newsletter para receber atualizações sobre novas resoluções, dicas de estudo e informações que vão fazer a diferença na sua preparação!